Chaque semaine, notre équipe de contrôle qualité 1 examine la documentation des fournisseurs pour les appareils de thérapie par ondes de choc. Une lacune récurrente se démarque : des données manquantes sur la sécurité cutanée normes de biocompatibilité ISO 10993 2. Cette négligence crée de réels problèmes pour les importateurs qui font ensuite face à des plaintes de clients, des retours, ou pire encore, des réclamations de responsabilité de la part des utilisateurs finaux subissant des réactions cutanées indésirables.
Oui, vous devriez absolument exiger un rapport de test de sécurité cutanée lors de l'approvisionnement en machines de thérapie par ondes de choc. Cette documentation, généralement basée sur les normes de biocompatibilité ISO 10993, prouve que les matériaux de l'appareil en contact avec la peau du patient ont été testés pour l'irritation, la toxicité et la sensibilisation, protégeant ainsi votre marque des problèmes réglementaires et des réclamations de responsabilité produit.
Laissez-moi vous expliquer exactement pourquoi cela est important pour votre entreprise, quels tests spécifiques exiger, et comment des données de sécurité vérifiées protègent vos bénéfices.
Pourquoi devrais-je exiger un rapport de test de sécurité cutanée avant de finaliser ma commande de machine à ondes de choc ?
Lorsque nous expédions appareils à ondes de choc 3 à des clients américains et européens, le premier document qu'ils demandent est la preuve de biocompatibilité. Il ne s'agit pas seulement de paperasse, cela représente une preuve vérifiée que chaque surface en contact avec la peau du patient a été scientifiquement évaluée pour sa sécurité.
Vous devriez exiger un rapport de test de sécurité cutanée car les pièces à main à ondes de choc entrent directement en contact avec la peau pendant le traitement, et les matériaux non testés peuvent provoquer une irritation, des réactions allergiques ou une toxicité. Cette documentation prouve que votre fournisseur a effectué des tests de biocompatibilité ISO 10993, essentiels pour la conformité réglementaire et la sécurité des patients.
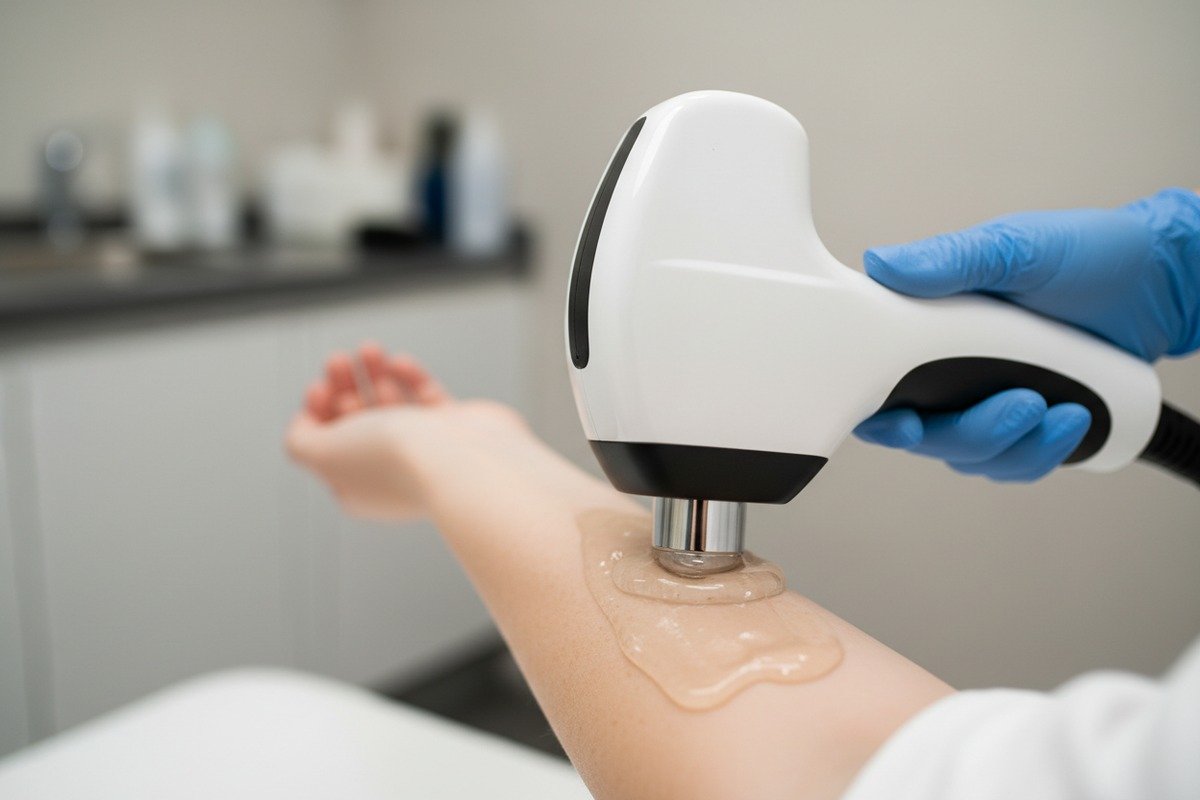
Que se passe-t-il lorsque les pièces à main touchent la peau
Les appareils de thérapie par ondes de choc délivrent de l'énergie acoustique 4 par le biais de pièces à main fermement pressées contre la peau du patient. Ces applicateurs contiennent des composants en plastique, en métal et en caoutchouc. Les gels de couplage appliqués entre la pièce à main et la peau introduisent une exposition chimique supplémentaire. Sans tests appropriés, l'un de ces matériaux pourrait libérer des substances nocives ou déclencher des réponses immunitaires.
Les réactions cutanées courantes dues à des appareils mal testés comprennent :
- Rougeur persistant au-delà de 48 heures
- Gonflement sur les sites de traitement
- Engourdissement dû à des dommages de pression
- Dermatite de contact due à des allergies aux matériaux
Notre équipe d'ingénierie a observé que les appareils utilisant des composés plastiques non vérifiés présentent souvent une dégradation de surface après des cycles de stérilisation répétés. Cette dégradation libère des microparticules qui entrent en contact avec la peau du patient lors des traitements ultérieurs.
Le cadre de test ISO 10993
Les Norme ISO 10993 5 fournit un cadre complet pour l'évaluation de la biocompatibilité des dispositifs médicaux. Pour les appareils à ondes de choc, les fournisseurs doivent fournir des preuves de ces tests spécifiques :
| Type de test | Ce qu'il mesure | Pourquoi c'est important pour les appareils à ondes de choc |
|---|---|---|
| Cytotoxicité (ISO 10993-5) | Mort cellulaire due aux substances lixiviables du matériau | Détecte les produits chimiques toxiques libérés par les plastiques de la pièce à main |
| Irritation (ISO 10993-10) | Réponse de rougeur et de gonflement de la peau | Confirme la sécurité de la surface de l'applicateur pour un contact répété |
| Sensibilisation (ISO 10993-10) | Potentiel de réaction allergique | Identifie les matériaux provoquant des réactions allergiques au fil du temps |
| Caractérisation des matériaux (ISO 10993-18) | Analyse de la composition chimique | Documente exactement quelles substances entrent en contact avec la peau du patient |
Considérations sur les ondes de choc radiales par rapport aux ondes de choc focalisées
Tous les appareils à ondes de choc ne présentent pas les mêmes risques. Les machines à ondes de pression radiales fonctionnent à des niveaux d'énergie plus bas avec des schémas de dispersion plus larges. Les appareils de thérapie par ondes de choc extracorporelles focalisées (ESWT) concentrent l'énergie dans des volumes tissulaires plus petits, ce qui exige une vérification de sécurité plus stricte.
Lors de l'achat de systèmes ESWT focalisés, demandez des données supplémentaires de cartographie de sortie acoustique en plus des rapports de sécurité cutanée. Cela confirme que la délivrance d'énergie reste dans des paramètres sûrs qui n'endommageront pas la peau par la chaleur.
Comment un rapport de sécurité m'aide-t-il à éviter les problèmes de responsabilité produit pour ma marque basée aux États-Unis ?
Nos clients américains nous disent constamment que les primes d'assurance responsabilité civile des produits dépendent fortement de la qualité de la documentation. Lorsque nous fournissons des rapports de sécurité complets avec nos machines, leurs assureurs reconnaissent des profils de risque plus faibles.
Un rapport de sécurité cutanée protège votre marque américaine contre les réclamations de responsabilité produit en fournissant des preuves documentées que vous avez fait preuve de diligence raisonnable dans la sélection des fournisseurs. Si un patient subit une réaction indésirable, cette documentation démontre que votre appareil répondait aux normes de sécurité reconnues, une défense essentielle contre les allégations de négligence.

Classification de la FDA et exigences en matière de documentation
La FDA classe les véritables machines de thérapie par ondes de choc comme des dispositifs médicaux de classe II 6 nécessitant une autorisation 510(k). Ce processus de notification préalable à la mise sur le marché exige des preuves substantielles de sécurité et d'efficacité, y compris des données de biocompatibilité conformes à la norme ISO 10993.
Voici ce que signifient réellement les différents statuts réglementaires pour votre exposition à la responsabilité :
| Statut réglementaire | Ce que cela signifie | Implications en matière de responsabilité |
|---|---|---|
| Autorisation 510(k) de la FDA | Dispositif examiné et autorisé pour des allégations médicales spécifiques | Protection solide contre la responsabilité ; preuves de sécurité documentées |
| Enregistré auprès de la FDA | Fabricant répertorié auprès de la FDA ; aucune évaluation de sécurité effectuée | Protection faible ; "enregistré" ne signifie pas "approuvé" |
| Aucun statut réglementaire aux États-Unis | L'appareil n'a pas été évalué par la FDA | Risque de responsabilité élevé ; difficile de se défendre contre les allégations de négligence |
Le piège de l" "enregistrement FDA"
De nombreux fournisseurs chinois commercialisent des appareils comme étant "enregistrés auprès de la FDA" pour suggérer leur légitimité. Cet enregistrement signifie simplement que le fabricant a répertorié son établissement et ses produits dans la base de données de la FDA. Il n'implique aucune évaluation de sécurité.
Lorsque nous préparons la documentation pour l'exportation vers les États-Unis, nous faisons clairement la distinction entre l'enregistrement et l'autorisation. Les appareils revendiquant des bénéfices thérapeutiques – régénération tissulaire, soulagement de la douleur, traitement de la fasciite – nécessitent légalement une autorisation 510(k), et non pas seulement un enregistrement.
Constitution de votre dossier de défense
Une défense efficace contre la responsabilité du fait des produits nécessite une chaîne de documentation prouvant que vous vous êtes approvisionné de manière responsable. Demandez ces documents avant de passer commande :
- Rapports de tests de biocompatibilité ISO 10993
- Spécifications des matériaux pour les surfaces en contact avec le patient
- Certification du système de management de la qualité ISO 13485 7
- Lettre d'autorisation FDA 510(k) (si usage médical revendiqué)
- Dossier de gestion des risques conformément à ISO 14971 8
Conservez ces documents de manière permanente. Si un litige survient des années après la vente, ces archives démontrent votre engagement envers la sécurité des patients.
Le coût réel de la documentation manquante
Envisagez un scénario où votre client salon signale plusieurs patients souffrant d'irritations cutanées persistantes après des traitements par ondes de choc. Sans documentation de biocompatibilité, vous ne pouvez pas prouver que les matériaux de l'appareil ont été testés comme étant sûrs. Les avocats des plaignants soutiendront que vous avez importé du matériel non testé, exposant ainsi les patients à des dommages prévisibles.
Les frais de défense seuls dépassent généralement 50 000 € avant tout règlement ou jugement. Une documentation de sécurité complète peut éviter ces situations entièrement.
Puis-je faire confiance au contrôle qualité de mon fournisseur s'il ne peut pas fournir de données vérifiées sur la sécurité de la peau ?
Dans notre usine, nous appliquons une règle simple : si nous ne pouvons pas le documenter, nous ne l'avons pas fait. Lorsque les fournisseurs prétendent que leurs appareils sont sûrs mais ne peuvent pas produire de rapports de test à l'appui, cela soulève de sérieuses questions sur l'ensemble de leur système qualité.
Non, vous ne pouvez pas faire confiance au contrôle qualité global d'un fournisseur s'il ne peut pas fournir de données vérifiées sur la sécurité de la peau. Les tests de biocompatibilité sont une exigence fondamentale pour la fabrication de dispositifs médicaux. Les fournisseurs qui manquent de cette documentation ont probablement des systèmes de gestion de la qualité inadéquats dans tous les processus de production.

Ce que révèle la documentation manquante
Un fournisseur qui ne peut pas fournir de rapports de test ISO 10993 vous dit quelque chose d'important sur son fonctionnement. Soit ils n'ont jamais effectué les tests requis, soit leurs systèmes de contrôle documentaire sont si désorganisés qu'ils ne peuvent pas localiser les enregistrements essentiels.
Les deux scénarios indiquent des problèmes de qualité systémiques. Si les tests de biocompatibilité ont été omis, quelles autres mesures de sécurité ont été négligées ? Si les enregistrements ne peuvent pas être localisés, comment ce fournisseur retracera-t-il les problèmes de production si des défauts apparaissent plus tard ?
Drapeaux rouges dans les réponses des fournisseurs
Lorsque nous évaluons des fournisseurs de composants potentiels, certaines réponses déclenchent immédiatement une préoccupation :
| Réponse du fournisseur | Ce que cela signifie probablement | Action recommandée |
|---|---|---|
| " Nos matériaux sont de qualité médicale, aucun test nécessaire " | Mauvaise compréhension des exigences réglementaires | Demander des certificats de test spécifiques |
| "Nous pouvons fournir des documents après votre commande" | Les documents peuvent ne pas exister ; création de rapports faux | Demander des rapports avant l'engagement d'achat |
| "Les clients précédents n'ont jamais demandé cela" | Lacunes du système qualité ; processus non testés | Envisager des fournisseurs alternatifs |
| "Les tests sont trop chers pour ce niveau de prix" | La réduction des coûts compromet la sécurité | Augmenter le budget ou accepter un risque plus élevé |
Évaluation des systèmes qualité des fournisseurs
Au-delà des rapports de sécurité cutanée, évaluez ces indicateurs de qualité lors de la qualification des fournisseurs de machines à ondes de choc :
Certification ISO 13485: Cette norme internationale spécifie les exigences de gestion de la qualité pour les organisations de dispositifs médicaux. Les fournisseurs certifiés maintiennent des procédures documentées pour le contrôle de la conception, la production et la surveillance post-marché.
Traçabilité de la fabrication: Les fournisseurs de qualité peuvent identifier les lots de matériaux exacts, les dates de production et les résultats des tests pour tout appareil par numéro de série. Cette traçabilité devient essentielle lors des situations de rappel.
Accès à l'historique des plaintes: Les fabricants réputés partagent des données agrégées de plaintes montrant les performances de l'appareil en utilisation réelle. Les schémas de plaintes liées à la peau indiquent des lacunes dans les tests.
Notre liste de contrôle de qualification des fournisseurs
Lorsque les clients demandent comment nous évaluons nos propres fournisseurs de composants, nous partageons ce processus de vérification :
- Demander le certificat ISO 13485 et vérifier auprès de l'organisme de certification
- Exiger des rapports de tests de biocompatibilité spécifiques aux composants en contact avec le patient
- Demander des certificats d'analyse de matériaux auprès des fournisseurs de matières premières
- Examiner les données de tendance des plaintes concernant les problèmes cutanés
- Mener un audit d'usine axé sur les systèmes de contrôle documentaire
Les fournisseurs qui réussissent les cinq points de contrôle démontrent un engagement qualité au-delà des assurances verbales.
Le fait d'exiger ces rapports de sécurité réduira-t-il le nombre de plaintes que je reçois de mes clients de salon ?
Notre équipe de service client suit les modèles de plaintes sur toutes les gammes de produits. Les données montrent une corrélation claire entre une documentation de sécurité complète et une réduction des plaintes sur le terrain. Les dispositifs dont la biocompatibilité est vérifiée surpassent systématiquement ceux qui présentent des lacunes documentaires.
Oui, exiger des rapports de sécurité cutanée réduira probablement les plaintes de vos clients de salon. Les appareils qui ont subi des tests de biocompatibilité appropriés connaissent moins de réactions cutanées indésirables, ce qui entraîne une plus grande satisfaction des patients et moins de plaintes liées au traitement auxquelles vos clients de salon doivent faire face.

Comprendre les causes profondes des plaintes
Les plaintes cutanées liées à la thérapie par ondes de choc entrent généralement dans ces catégories :
Réactions immédiates: Rougeur excessive, gonflement ou sensation de brûlure pendant le traitement. Souvent causé par des gels de couplage non testés ou des matériaux de surface de pièce à main qui irritent la peau sensible.
Réactions retardées: Dermatite de contact apparaissant 24 à 72 heures après le traitement. Indique généralement une sensibilisation aux composants du matériau, ce que les tests ISO 10993-10 détecteraient.
Effets cumulatifs: Changements cutanés se développant après plusieurs séances de traitement. Les données de biocompatibilité à long terme aident à prédire ces réponses avant qu'elles n'affectent les patients de vos clients.
Comment des tests appropriés préviennent les plaintes
Lorsque les fournisseurs effectuent des tests de biocompatibilité complets, ils identifient les matériaux problématiques avant la production. Cette approche proactive élimine les sources de plaintes plutôt que de réagir aux défaillances sur le terrain.
| Type de plainte | Test qui le prévient | Réduction attendue |
|---|---|---|
| Irritation cutanée pendant le traitement | Tests d'irritation (ISO 10993-10) | 70-80% |
| Réactions allergiques post-traitement | Tests de sensibilisation (ISO 10993-10) | 60-70% |
| Changements inhabituels de la texture de la peau | Tests de cytotoxicité (ISO 10993-5) | 50-60% |
| Réactions cutanées liées au gel | Caractérisation des matériaux (ISO 10993-18) | 80-90% |
Soutenir vos clients de salon
Au-delà de la réduction de la fréquence des plaintes, la documentation de sécurité aide vos clients de salon à réagir efficacement lorsque des problèmes surviennent. Leur fournir des résumés de tests de biocompatibilité permet des conversations éclairées avec les patients préoccupés.
Les salons peuvent expliquer que les appareils ont subi une évaluation de sécurité rigoureuse et que des réactions temporaires légères entrent dans les paramètres normaux documentés lors des tests cliniques. Cette transparence renforce la confiance des patients et réduit les escalades vers des plaintes formelles.
Tendances actuelles de l'industrie
La Société Internationale de Traitement par Ondes de Choc Médicales (ISMST) a mis à jour ses directives en soulignant l'inspection cutanée post-traitement. Les praticiens doivent surveiller les schémas de rougeur qui peuvent indiquer des problèmes d'appareil. Cette surveillance accrue rend la documentation de sécurité vérifiée plus précieuse que jamais.
Nous observons une demande croissante de " fiches récapitulatives de biocompatibilité " — des documents d'une page condensant les rapports de test complets dans des formats conviviaux pour les praticiens. Ces résumés aident le personnel du salon à comprendre quels tests ont été effectués sans avoir à examiner les rapports techniques de laboratoire.
Impact Commercial à Long Terme
La réduction des plaintes protège la réputation de votre marque et renforce les relations avec les clients. Les propriétaires de salons qui reçoivent moins de plaintes de patients restent des clients fidèles. Ils deviennent également des sources de référence, recommandant vos appareils à leurs collègues en fonction de performances fiables.
Le coût des tests de sécurité complets lors de l'approvisionnement est minime par rapport à la gestion des escalades de plaintes, au traitement des retours et à la reconstruction de relations commerciales endommagées.
Conclusion
Exiger des rapports de tests de sécurité cutanée lors de l'approvisionnement en machines de thérapie par ondes de choc protège votre marque, réduit l'exposition à la responsabilité et garantit de meilleurs résultats pour les utilisateurs finaux. Cette documentation n'est pas facultative — elle est essentielle pour une importation responsable et un succès commercial à long terme.
Notes de bas de page
1. Explique le rôle essentiel du contrôle qualité pour garantir la sécurité et l'efficacité des dispositifs médicaux. ︎
2. Fournit un aperçu des normes internationales pour l'évaluation de la biocompatibilité des dispositifs médicaux. ︎
3. Fournit un aperçu complet de la thérapie par ondes de choc extracorporelles et de ses utilisations médicales. ︎
4. Définit l'énergie acoustique comme une forme de son utilisée dans le diagnostic et la thérapeutique médicaux. ︎
5. Explique que l'ISO 10993 est la norme clé et le cadre complet pour les tests de biocompatibilité des dispositifs médicaux. ︎
6. Définit les dispositifs médicaux de classe II de la FDA comme des produits à risque modéré nécessitant des contrôles spéciaux pour la sécurité et l'efficacité. ︎
7. Remplacé par une page de travail du BSI, un organisme de certification faisant autorité, détaillant la certification ISO 13485. ︎
8. Remplacé par la page officielle de la boutique en ligne de l'IEC pour la norme ISO 14971. ︎


