Jede Woche inspiziert unser Qualitätskontrollteam 1 prüft Lieferantendokumentation für Stoßwellentherapiegeräte. Eine wiederkehrende Lücke sticht hervor: fehlende Hautsicherheitsdaten ISO 10993 Biokompatibilitätsstandards 2. Diese Nachlässigkeit schafft echte Probleme für Importeure, die später mit Kundenbeschwerden, Rücksendungen oder schlimmer noch – Haftungsansprüchen von Endverbrauchern konfrontiert werden, die unerwünschte Hautreaktionen erfahren.
Ja, Sie sollten unbedingt einen Hautverträglichkeitsbericht verlangen, wenn Sie Stoßwellentherapiegeräte beschaffen. Diese Dokumentation, die in der Regel auf den ISO 10993 Biokompatibilitätsstandards basiert, beweist, dass die Materialien des Geräts, die mit der Patientenhaut in Kontakt kommen, auf Reizung, Toxizität und Sensibilisierung getestet wurden – und schützt Ihre Marke vor regulatorischen Problemen und Produkthaftungsansprüchen.
Lassen Sie mich Ihnen genau erklären, warum das für Ihr Unternehmen wichtig ist, welche spezifischen Tests Sie verlangen sollten und wie verifizierte Sicherheitsdaten Ihre Rentabilität schützen.
Warum sollte ich einen Hautsicherheitsprüfbericht anfordern, bevor ich meine Stoßwellenmaschinenbestellung abschließe?
Wenn wir versenden Stoßwellengeräte 3 an US-amerikanische und europäische Kunden, ist das erste Dokument, das sie anfordern, ein Nachweis der Biokompatibilität. Dies ist nicht nur Papierkram – es stellt einen verifizierten Beweis dar, dass jede Oberfläche, die die Patientenhaut berührt, wissenschaftlich auf Sicherheit geprüft wurde.
Sie sollten einen Hautverträglichkeitsbericht verlangen, da Stoßwellen-Handstücke während der Behandlung direkten Hautkontakt haben und nicht getestete Materialien Reizungen, allergische Reaktionen oder Toxizität verursachen können. Diese Dokumentation beweist, dass Ihr Lieferant die ISO 10993-Biokompatibilitätstests durchgeführt hat, was für die Einhaltung von Vorschriften und die Patientensicherheit unerlässlich ist.
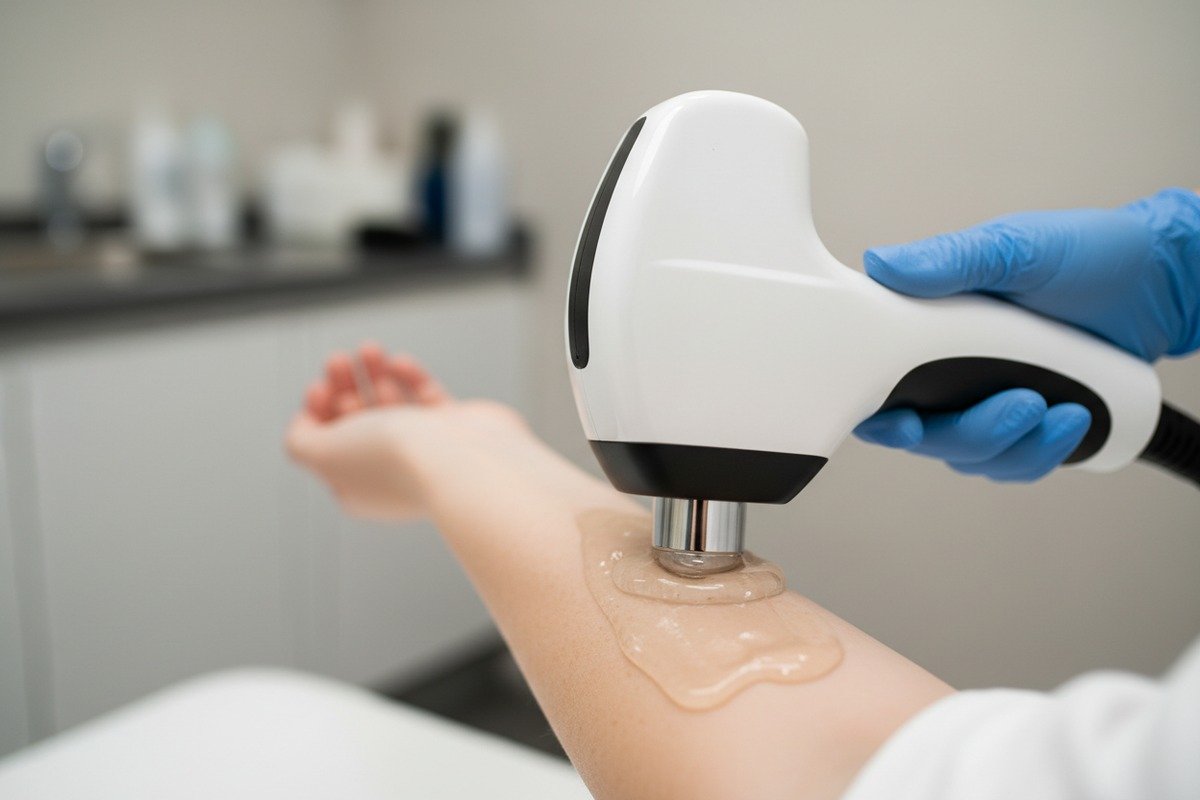
Was passiert, wenn Handstücke die Haut berühren
Stoßwellentherapiegeräte liefern akustische Energie 4 durch Handstücke, die fest auf die Haut des Patienten gedrückt werden. Diese Applikatoren enthalten Kunststoffe, Metalle und Gummikomponenten. Zwischen Handstück und Haut aufgetragene Kopplungsgels führen zu zusätzlicher chemischer Belastung. Ohne ordnungsgemäße Prüfung könnten alle diese Materialien schädliche Substanzen abgeben oder Immunreaktionen auslösen.
Häufige Hautreaktionen von schlecht getesteten Geräten sind:
- Rötung, die länger als 48 Stunden anhält
- Schwellung an den Behandlungsstellen
- Taubheit durch Druckschäden
- Kontaktdermatitis durch Materialallergien
Unser Ingenieurteam hat beobachtet, dass Geräte, die nicht verifizierte Kunststoffverbindungen verwenden, nach wiederholten Sterilisationszyklen oft Oberflächenabbau zeigen. Dieser Abbau setzt Mikropartikel frei, die während nachfolgender Behandlungen Hautkontakt mit dem Patienten haben.
Der ISO 10993 Testrahmen
Die ISO 10993 Standard 5 bietet einen umfassenden Rahmen für die Bewertung der Biokompatibilität von Medizinprodukten. Für Stoßwellengeräte sollten Lieferanten Nachweise für diese spezifischen Tests erbringen:
| Testtyp | Was es misst | Warum es für Stoßwellengeräte wichtig ist |
|---|---|---|
| Zytotoxizität (ISO 10993-5) | Zelltod durch auslaugbare Materialien | Erkennt toxische Chemikalien, die aus Handstückkunststoffen freigesetzt werden |
| Reizung (ISO 10993-10) | Hautrötung und Schwellungsreaktion | Bestätigt die Sicherheit der Applikatoroberfläche für wiederholten Kontakt |
| Sensibilisierung (ISO 10993-10) | Potenzial für allergische Reaktionen | Identifiziert Materialien, die im Laufe der Zeit allergische Reaktionen hervorrufen |
| Materialcharakterisierung (ISO 10993-18) | Analyse der chemischen Zusammensetzung | Dokumentiert genau, welche Substanzen die Haut des Patienten berühren |
Überlegungen zu radialen vs. fokussierten Stoßwellen
Nicht alle Stoßwellengeräte bergen das gleiche Risiko. Radialdruckwellengeräte arbeiten mit geringeren Energieniveaus und breiteren Streumustern. Fokussierte extrakorporale Stoßwellentherapie (ESWT)-Geräte konzentrieren die Energie auf kleinere Gewebevolumina, was eine strengere Sicherheitsüberprüfung erfordert.
Fordern Sie bei der Beschaffung von fokussierten ESWT-Systemen zusätzlich akustische Ausgangsmapping-Daten neben Hautsicherheitsberichten an. Dies bestätigt, dass die Energieabgabe innerhalb sicherer Parameter bleibt, die keine thermischen Hautschäden verursachen.
Wie hilft mir ein Sicherheitsbericht, Produkthaftungsprobleme für meine in den USA ansässige Marke zu vermeiden?
Unsere US-Kunden teilen uns immer wieder mit, dass die Prämien für Produkthaftpflichtversicherungen stark von der Qualität der Dokumentation abhängen. Wenn wir umfassende Sicherheitsberichte für unsere Geräte liefern, erkennen ihre Versicherer geringere Risikoprofile.
Ein Hautsicherheitsbericht schützt Ihre US-Marke vor Produkthaftungsansprüchen, indem er dokumentierte Beweise dafür liefert, dass Sie bei der Lieferantenauswahl gebührend Sorgfalt walten ließen. Wenn ein Patient eine unerwünschte Reaktion erfährt, belegt diese Dokumentation, dass Ihr Gerät anerkannte Sicherheitsstandards erfüllte – eine entscheidende Verteidigung gegen Fahrlässigkeitsvorwürfe.

FDA-Klassifizierung und Dokumentationsanforderungen
Die FDA klassifiziert echte Stoßwellentherapiegeräte als Medizinprodukte der Klasse II 6 die eine 510(k)-Zulassung erfordern. Dieses Vorabgenehmigungsverfahren erfordert erhebliche Nachweise für Sicherheit und Wirksamkeit, einschließlich Biokompatibilitätsdaten gemäß ISO 10993.
Hier ist, was verschiedene regulatorische Status tatsächlich für Ihre Haftungsexposition bedeuten:
| Regulatorischer Status | Was es bedeutet | Haftungsfolgen |
|---|---|---|
| FDA 510(k) zugelassen | Gerät überprüft und für spezifische medizinische Ansprüche freigegeben | Starker Haftungsschutz; dokumentierte Sicherheitsnachweise |
| FDA-registriert | Hersteller bei der FDA gelistet; keine Sicherheitsprüfung durchgeführt | Schwacher Schutz; "registriert" bedeutet nicht "genehmigt" |
| Kein US-Regulierungsstatus | Gerät wurde nicht von der FDA bewertet | Hohes Haftungsrisiko; schwierige Verteidigung von Fahrlässigkeitsansprüchen |
Die "FDA Registered"-Falle
Viele chinesische Lieferanten vermarkten Geräte als "FDA registered", um Legitimität vorzutäuschen. Diese Registrierung bedeutet lediglich, dass der Hersteller seine Einrichtung und Produkte in der FDA-Datenbank aufgeführt hat. Sie beinhaltet keinerlei Sicherheitsbewertung.
Wenn wir Dokumentationen für den US-Export vorbereiten, unterscheiden wir klar zwischen Registrierung und Freigabe. Geräte, die therapeutische Vorteile beanspruchen – Geweberegeneration, Schmerzlinderung, Behandlung von Fasziitis – benötigen gesetzlich eine 510(k)-Freigabe, nicht nur eine Registrierung.
Aufbau Ihrer Verteidigungsakte
Eine effektive Produkthaftungsverteidigung erfordert eine Dokumentationskette, die beweist, dass Sie verantwortungsvoll beschafft haben. Fordern Sie diese Dokumente vor der Auftragserteilung an:
- ISO 10993 Biokompatibilitätstestberichte
- Materialspezifikationen für patientenkontaktierte Oberflächen
- ISO 13485 Qualitätsmanagement-Zertifizierung 7
- FDA 510(k) Freigabebrief (bei Beanspruchung medizinischer Nutzung)
- Risikomanagementakte gemäß ISO 14971 8
Bewahren Sie diese Dokumente dauerhaft auf. Sollte es Jahre nach dem Verkauf zu einem Rechtsstreit kommen, beweist dieses Archiv Ihr Engagement für die Patientensicherheit.
Die wahren Kosten fehlender Dokumentation
Stellen Sie sich ein Szenario vor, in dem Ihr Salonkunde nach Stoßwellenbehandlungen über mehrere Patienten mit anhaltenden Hautreizungen berichtet. Ohne Biokompatibilitätsdokumentation können Sie nicht nachweisen, dass die Gerätematerialien auf Sicherheit getestet wurden. Klägeranwälte werden argumentieren, dass Sie ungetestete Geräte importiert haben und damit Patienten vorhersehbarem Schaden ausgesetzt haben.
Allein die Verteidigungskosten übersteigen in der Regel 50.000 US-Dollar, bevor es zu einer Einigung oder einem Urteil kommt. Umfassende Sicherheitsdokumentation kann diese Situationen gänzlich verhindern.
Kann ich der Qualitätskontrolle meines Lieferanten vertrauen, wenn er keine verifizierten Hautsicherheitsdaten vorlegen kann?
In unserer Fabrik halten wir uns an eine einfache Regel: Was wir nicht dokumentieren können, haben wir nicht getan. Wenn Lieferanten behaupten, ihre Geräte seien sicher, aber keine unterstützenden Testberichte vorlegen können, wirft dies ernsthafte Fragen zu ihrem gesamten Qualitätssystem auf.
Nein, Sie können der allgemeinen Qualitätskontrolle eines Lieferanten nicht vertrauen, wenn dieser keine verifizierten Daten zur Hautverträglichkeit vorlegen kann. Biokompatibilitätstests sind eine grundlegende Anforderung für die Herstellung von Medizinprodukten. Lieferanten, denen diese Dokumentation fehlt, verfügen wahrscheinlich über unzureichende Qualitätsmanagementsysteme für alle Produktionsprozesse.

Was fehlende Dokumentation offenbart
Ein Lieferant, der keine ISO 10993-Testberichte vorlegen kann, sagt Ihnen etwas Wichtiges über seinen Betrieb. Entweder haben sie die erforderlichen Tests nie durchgeführt, oder ihre Dokumentenmanagementsysteme sind so unorganisiert, dass sie wesentliche Aufzeichnungen nicht finden können.
Beide Szenarien deuten auf systemische Qualitätsprobleme hin. Wenn Biokompatibilitätstests übersprungen wurden, welche anderen Sicherheitsschritte wurden weggelassen? Wenn Aufzeichnungen nicht gefunden werden können, wie wird dieser Lieferant Produktionsprobleme nachverfolgen, wenn später Mängel auftreten?
Warnsignale in Lieferantenantworten
Wenn wir potenzielle Komponentenlieferanten bewerten, lösen bestimmte Antworten sofort Bedenken aus:
| Antwort des Lieferanten | Was es wahrscheinlich bedeutet | Empfohlene Maßnahme |
|---|---|---|
| "Unsere Materialien sind medizinischer Qualität – keine Tests erforderlich" | Missverständnis der regulatorischen Anforderungen | Fordern Sie spezifische Testzertifikate an. |
| "Wir können Dokumente nach Ihrer Bestellung bereitstellen" | Dokumente existieren möglicherweise nicht; Erstellung falscher Berichte | Berichte vor Kaufzusage verlangen |
| "Frühere Kunden haben dies nie verlangt" | Lücken im Qualitätssystem; ungetestete Prozesse | Alternative Lieferanten in Betracht ziehen |
| "Tests sind für diesen Preis zu teuer" | Kosteneinsparungen beeinträchtigen die Sicherheit | Budget erhöhen oder höheres Risiko akzeptieren |
Bewertung von Lieferantenqualitätssystemen
Über Hautsicherheitsberichte hinaus bewerten Sie diese Qualitätsindikatoren bei der Qualifizierung von Stoßwellenmaschinenlieferanten:
ISO 13485-Zertifizierung: Dieser internationale Standard legt Anforderungen an das Qualitätsmanagement für Organisationen im Bereich Medizinprodukte fest. Zertifizierte Lieferanten unterhalten dokumentierte Verfahren für Designkontrolle, Produktion und Überwachung nach dem Inverkehrbringen.
Rückverfolgbarkeit der Fertigung: Qualitätslieferanten können anhand der Seriennummer genaue Materialchargen, Produktionsdaten und Testergebnisse für jedes Gerät identifizieren. Diese Rückverfolgbarkeit wird in Rückrufsituationen kritisch.
Zugriff auf Beschwerdehistorie: Seriöse Hersteller teilen aggregierte Beschwerdedaten, die die Geräteleistung im realen Einsatz zeigen. Muster von hautbezogenen Beschwerden deuten auf Testlücken hin.
Unsere Checkliste zur Lieferantenqualifizierung
Wenn Kunden fragen, wie wir unsere eigenen Komponentenlieferanten bewerten, teilen wir diesen Verifizierungsprozess mit:
- Anforderung des ISO 13485-Zertifikats und Überprüfung bei der Zertifizierungsstelle
- Forderung nach Biokompatibilitätstestberichten, die sich speziell auf patientenkontaktierende Komponenten beziehen
- Anforderung von Materialanalysenzertifikaten von Rohstofflieferanten
- Überprüfung von Beschwerdetrenddaten für hautbezogene Probleme
- Durchführung von Werksaudits mit Schwerpunkt auf Dokumentenmanagementsystemen
Lieferanten, die alle fünf Prüfpunkte bestehen, zeigen ein Qualitätsengagement, das über mündliche Zusicherungen hinausgeht.
Wird die Anforderung dieser Sicherheitsberichte die Anzahl der Beschwerden reduzieren, die ich von meinen Salonkunden erhalte?
Unser Kundenservice-Team verfolgt Beschwerdemuster über alle Produktlinien hinweg. Die Daten zeigen eine klare Korrelation zwischen umfassender Sicherheitsdokumentation und reduzierten Feld-Beschwerden. Geräte mit verifizierter Biokompatibilität übertreffen durchweg diejenigen mit Dokumentationslücken.
Ja, die Anforderung von Hautsicherheitsberichten wird wahrscheinlich die Beschwerden Ihrer Salonkunden reduzieren. Geräte, die ordnungsgemäß auf Biokompatibilität getestet wurden, weisen weniger unerwünschte Hautreaktionen auf, was zu einer höheren Patientenzufriedenheit und weniger behandlungsbedingten Beschwerden führt, mit denen sich Ihre Salonkunden auseinandersetzen müssen.

Verständnis der Ursachen von Beschwerden
Hautbezogene Beschwerden bei der Stoßwellentherapie fallen typischerweise in diese Kategorien:
Sofortige Reaktionen: Übermäßige Rötung, Schwellung oder Brennen während der Behandlung. Oft verursacht durch ungetestete Kopplungsgels oder Oberflächenmaterialien des Handstücks, die empfindliche Haut reizen.
Verzögerte Reaktionen: Kontaktdermatitis, die 24-72 Stunden nach der Behandlung auftritt. Zeigt normalerweise eine Sensibilisierung gegenüber Materialkomponenten an – genau das, was die ISO 10993-10-Prüfung erkennen würde.
Kumulative Effekte: Hautveränderungen, die sich nach mehreren Behandlungssitzungen entwickeln. Langfristige Daten zur Biokompatibilität helfen, diese Reaktionen vorherzusagen, bevor sie die Patienten Ihrer Kunden beeinträchtigen.
Wie ordnungsgemäße Tests Beschwerden verhindern
Wenn Lieferanten umfassende Biokompatibilitätstests durchführen, identifizieren sie problematische Materialien vor der Produktion. Dieser proaktive Ansatz eliminiert Beschwerdequellen, anstatt auf Ausfälle im Feld zu reagieren.
| Beschwerdetyp | Tests, die dies verhindern | Erwartete Reduzierung |
|---|---|---|
| Hautreizung während der Behandlung | Reizungstest (ISO 10993-10) | 70-80% |
| Allergische Reaktionen nach der Behandlung | Sensibilisierungstest (ISO 10993-10) | 60-70% |
| Ungewöhnliche Hauttexturveränderungen | Zytotoxizitätstest (ISO 10993-5) | 50-60% |
| Gelbedingte Hautreaktionen | Materialcharakterisierung (ISO 10993-18) | 80-90% |
Unterstützung Ihrer Salonkunden
Über die Reduzierung der Beschwerdehäufigkeit hinaus hilft die Sicherheitsdokumentation Ihren Salonkunden, effektiv zu reagieren, wenn Probleme auftreten. Die Bereitstellung von Zusammenfassungen von Biokompatibilitätstests ermöglicht informierte Gespräche mit besorgten Patienten.
Salons können erklären, dass die Geräte einer strengen Sicherheitsbewertung unterzogen wurden und dass leichte vorübergehende Reaktionen innerhalb der normalen Parameter liegen, die während klinischer Tests dokumentiert wurden. Diese Transparenz schafft Vertrauen bei den Patienten und reduziert die Eskalation zu formellen Beschwerden.
Aktuelle Branchentrends
Die International Society for Medical Shockwave Treatment (ISMST) hat ihre Richtlinien aktualisiert und betont die Inspektion der Haut nach der Behandlung. Praktiker sollten auf Rötungsmuster achten, die auf Geräteprobleme hinweisen können. Diese erhöhte Überprüfung macht verifizierte Sicherheitsdokumentationen wertvoller als je zuvor.
Wir beobachten eine wachsende Nachfrage nach "Biokompatibilitäts-Zusammenfassungsblättern" – einseitigen Dokumenten, die vollständige Testberichte in praxisorientierte Formate zusammenfassen. Diese Zusammenfassungen helfen dem Salonpersonal zu verstehen, welche Tests durchgeführt wurden, ohne technische Laborberichte durchsehen zu müssen.
Langfristige Geschäftsauswirkungen
Die Reduzierung von Beschwerden schützt Ihren Markenruf und stärkt die Kundenbeziehungen. Salonbesitzer, die weniger Patientenbeschwerden haben, bleiben loyale Kunden. Sie werden auch zu Empfehlungsquellen und empfehlen Ihre Geräte aufgrund zuverlässiger Leistung an Kollegen weiter.
Die Kosten für umfassende Sicherheitstests während der Beschaffung sind minimal im Vergleich zur Bewältigung von Beschwerdeeskalationen, der Bearbeitung von Rücksendungen und dem Wiederaufbau beschädigter Geschäftsbeziehungen.
Schlussfolgerung
Die Anforderung von Hautsicherheitstestberichten bei der Beschaffung von Stoßwellentherapiegeräten schützt Ihre Marke, reduziert die Haftung und gewährleistet bessere Ergebnisse für Endverbraucher. Diese Dokumentation ist nicht optional – sie ist unerlässlich für verantwortungsvolle Importe und langfristigen Geschäftserfolg.
Fußnoten
1. Erklärt die entscheidende Rolle der Qualitätskontrolle bei der Gewährleistung der Sicherheit und Wirksamkeit von Medizinprodukten. ︎
2. Bietet einen Überblick über die internationalen Standards zur Bewertung der Biokompatibilität von Medizinprodukten. ︎
3. Bietet einen umfassenden Überblick über die extrakorporale Stoßwellentherapie und ihre medizinischen Anwendungen. ︎
4. Definiert akustische Energie als eine Form von Schall, die in der medizinischen Diagnostik und Therapie eingesetzt wird. ︎
5. Erklärt die ISO 10993 als den Schlüsselstandard und umfassenden Rahmen für die Biokompatibilitätstests von Medizinprodukten. ︎
6. Definiert FDA-Medizinprodukte der Klasse II als Produkte mit mittlerem Risiko, die spezielle Kontrollen für Sicherheit und Wirksamkeit erfordern. ︎
7. Ersetzt durch eine Arbeitsseite von BSI, einer maßgeblichen Zertifizierungsstelle, die die ISO 13485-Zertifizierung detailliert beschreibt. ︎
8. Ersetzt durch die offizielle Seite des IEC Webstores für den ISO 14971-Standard. ︎


