Cada semana, nuestro equipo de control de calidad 1 revisa la documentación del proveedor para máquinas de terapia de ondas de choque. Un vacío recurrente se destaca: falta de datos de seguridad para la piel normas de biocompatibilidad ISO 10993 2. Esta omisión crea problemas reales para los importadores que luego se enfrentan a quejas de clientes, devoluciones o, lo que es peor, reclamaciones de responsabilidad de los usuarios finales que experimentan reacciones adversas en la piel.
Sí, definitivamente debes exigir un informe de prueba de seguridad cutánea al adquirir máquinas de terapia de ondas de choque. Esta documentación, generalmente basada en los estándares de biocompatibilidad ISO 10993, demuestra que los materiales del dispositivo que entran en contacto con la piel del paciente han sido probados para detectar irritación, toxicidad y sensibilización, protegiendo tu marca de problemas regulatorios y reclamaciones de responsabilidad del producto.
Permítame explicarle exactamente por qué esto es importante para su negocio, qué pruebas específicas debe exigir y cómo los datos de seguridad verificados protegen sus beneficios.
¿Por qué debería exigir un informe de prueba de seguridad de la piel antes de finalizar mi pedido de máquina de ondas de choque?
Cuando enviamos dispositivos de ondas de choque 3 a clientes de EE. UU. y Europa, el primer documento que solicitan es la evidencia de biocompatibilidad. Esto no es solo papeleo, representa una prueba verificada de que cada superficie que entra en contacto con la piel del paciente ha sido evaluada científicamente para garantizar su seguridad.
Debe exigir un informe de prueba de seguridad de la piel porque las piezas de mano de ondas de choque entran en contacto directo con la piel durante el tratamiento, y los materiales no probados pueden causar irritación, reacciones alérgicas o toxicidad. Esta documentación demuestra que su proveedor ha realizado pruebas de biocompatibilidad ISO 10993, que son esenciales para el cumplimiento normativo y la seguridad del paciente.
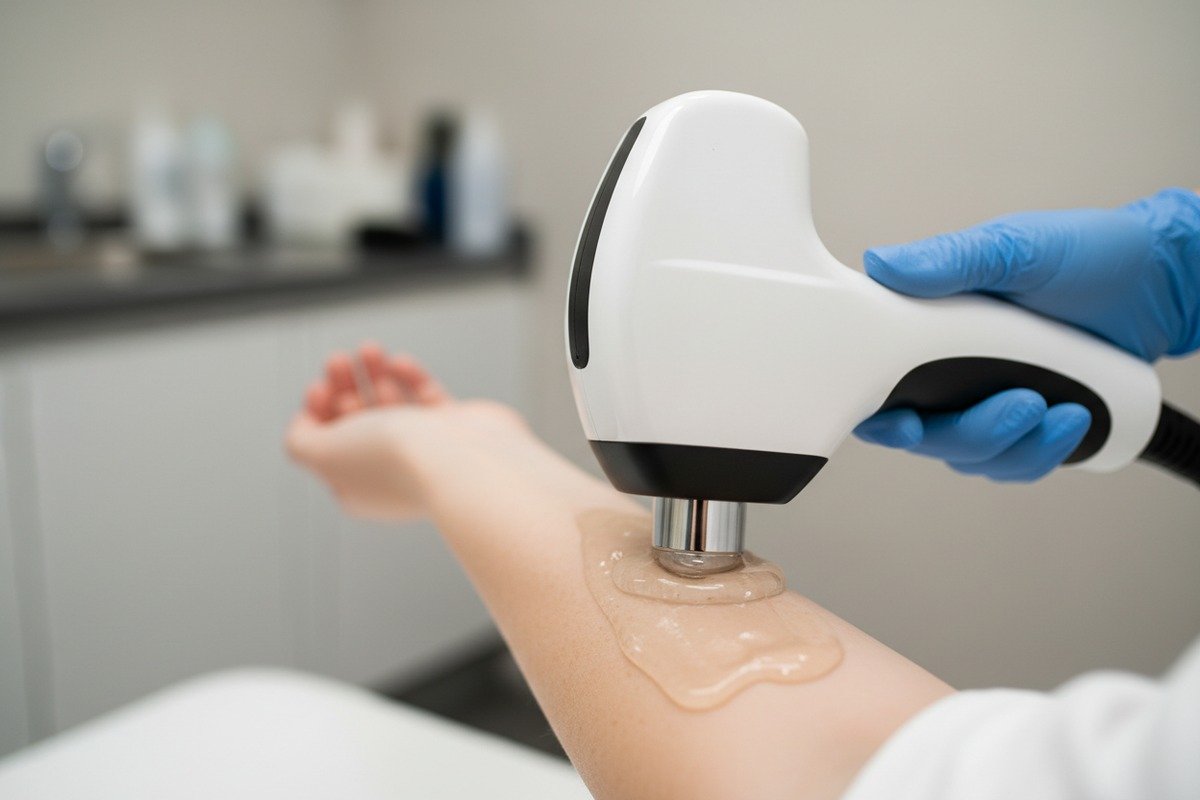
Qué sucede cuando las piezas de mano tocan la piel
Las máquinas de terapia de ondas de choque entregan energía acústica 4 a través de piezas de mano presionadas firmemente contra la piel del paciente. Estos aplicadores contienen plásticos, metales y componentes de caucho. Los geles de acoplamiento aplicados entre la pieza de mano y la piel introducen una exposición química adicional. Sin pruebas adecuadas, cualquiera de estos materiales podría liberar sustancias nocivas o desencadenar respuestas inmunitarias.
Las reacciones cutáneas comunes de los dispositivos mal probados incluyen:
- Enrojecimiento que dura más de 48 horas
- Hinchazón en los sitios de tratamiento
- Entumecimiento por daño por presión
- Dermatitis de contacto por alergias a materiales
Nuestro equipo de ingeniería ha observado que los dispositivos que utilizan compuestos plásticos no verificados a menudo muestran degradación superficial después de ciclos de esterilización repetidos. Esta degradación libera micropartículas que entran en contacto con la piel del paciente durante tratamientos posteriores.
El Marco de Pruebas ISO 10993
El Norma ISO 10993 5 proporciona un marco integral para evaluar la biocompatibilidad de los dispositivos médicos. Para las máquinas de ondas de choque, los proveedores deben proporcionar evidencia de estas pruebas específicas:
| Tipo de prueba | Qué mide | Por qué es importante para los dispositivos de ondas de choque |
|---|---|---|
| Citotoxicidad (ISO 10993-5) | Muerte celular por lixiviables del material | Detecta productos químicos tóxicos liberados de los plásticos de las piezas de mano |
| Irritación (ISO 10993-10) | Respuesta de enrojecimiento e hinchazón de la piel | Confirma la seguridad de la superficie del aplicador para contacto repetido |
| Sensibilización (ISO 10993-10) | Potencial de reacción alérgica | Identifica materiales que causan respuestas alérgicas con el tiempo |
| Caracterización de materiales (ISO 10993-18) | Análisis de composición química | Documenta exactamente qué sustancias entran en contacto con la piel del paciente |
Consideraciones sobre ondas de choque radiales vs. enfocadas
No todos los dispositivos de ondas de choque conllevan el mismo riesgo. Las máquinas de ondas de presión radial operan a niveles de energía más bajos con patrones de dispersión más amplios. Los dispositivos de terapia de ondas de choque extracorpóreas enfocadas (ESWT) concentran la energía en volúmenes de tejido más pequeños, lo que exige una verificación de seguridad más estricta.
Al adquirir sistemas ESWT enfocados, solicite datos adicionales de mapeo de salida acústica junto con informes de seguridad cutánea. Esto confirma que la entrega de energía se mantiene dentro de parámetros seguros que no causarán daño térmico a la piel.
¿Cómo me ayuda un informe de seguridad a evitar problemas de responsabilidad de producto para mi marca con sede en EE. UU.?
Nuestros clientes de EE. UU. nos dicen constantemente que las primas del seguro de responsabilidad civil del producto dependen en gran medida de la calidad de la documentación. Cuando proporcionamos informes de seguridad completos con nuestras máquinas, sus aseguradoras reconocen perfiles de riesgo más bajos.
Un informe de seguridad de la piel protege su marca estadounidense de reclamaciones de responsabilidad por productos al proporcionar evidencia documentada de que ejerció la debida diligencia en la selección de proveedores. Si un paciente experimenta una reacción adversa, esta documentación demuestra que su dispositivo cumplió con los estándares de seguridad reconocidos, una defensa crítica contra las acusaciones de negligencia.

Clasificación de la FDA y requisitos de documentación
La FDA clasifica las verdaderas máquinas de terapia de ondas de choque como dispositivos médicos de Clase II 6 que requieren la autorización 510(k). Este proceso de notificación previa a la comercialización exige pruebas sustanciales de seguridad y eficacia, incluidos datos de biocompatibilidad según la norma ISO 10993.
Aquí se explica lo que significan realmente los diferentes estados regulatorios para su exposición a la responsabilidad civil:
| Estado regulatorio | Qué significa | Implicaciones de responsabilidad |
|---|---|---|
| Autorizado por la FDA 510(k) | Dispositivo revisado y autorizado para reclamaciones médicas específicas | Fuerte protección de responsabilidad; evidencia de seguridad documentada |
| Registrado por la FDA | Fabricante listado con la FDA; no se realizó revisión de seguridad | Protección débil; "registrado" no significa "aprobado" |
| Sin estatus regulatorio en EE. UU. | El dispositivo no ha sido evaluado por la FDA | Alto riesgo de responsabilidad; difícil de defender reclamaciones por negligencia |
La trampa del "Registrado por la FDA"
Muchos proveedores chinos comercializan dispositivos como "registrados por la FDA" para sugerir legitimidad. Este registro simplemente significa que el fabricante ha listado sus instalaciones y productos en la base de datos de la FDA. Implica cero evaluación de seguridad.
Cuando preparamos la documentación para la exportación a EE. UU., distinguimos claramente entre registro y autorización. Los dispositivos que reclaman beneficios terapéuticos (regeneración de tejidos, alivio del dolor, tratamiento de la fascitis) requieren legalmente la autorización 510(k), no solo el registro.
Construyendo su archivo de defensa
Una defensa eficaz de la responsabilidad del producto requiere una cadena de documentación que demuestre que usted se abasteció de manera responsable. Solicite estos documentos antes de realizar pedidos:
- Informes de pruebas de biocompatibilidad ISO 10993
- Especificaciones de materiales para superficies de contacto con el paciente
- Certificación de gestión de calidad ISO 13485 7
- Carta de autorización FDA 510(k) (si se reclama uso médico)
- Archivo de gestión de riesgos según ISO 14971 8
Almacene estos documentos de forma permanente. Si surge un litigio años después de la venta, este archivo demuestra su compromiso con la seguridad del paciente.
Costo real de la documentación faltante
Considere un escenario en el que su cliente de salón informa que varios pacientes presentan irritación persistente en la piel después de tratamientos de ondas de choque. Sin documentación de biocompatibilidad, no puede probar que los materiales del dispositivo se probaron como seguros. Los abogados demandantes argumentarán que importó equipos no probados, exponiendo a los pacientes a daños previsibles.
Los costos de defensa por sí solos suelen superar los 50.000 USD antes de cualquier acuerdo o sentencia. La documentación de seguridad integral puede prevenir estas situaciones por completo.
¿Puedo confiar en el control de calidad de mi proveedor si no pueden proporcionar datos verificados sobre la seguridad de la piel?
En nuestra fábrica, mantenemos una regla simple: si no podemos documentarlo, no lo hicimos. Cuando los proveedores afirman que sus dispositivos son seguros pero no pueden producir informes de prueba de respaldo, esto plantea serias dudas sobre todo su sistema de calidad.
No, no puede confiar en el control de calidad general de un proveedor si no puede proporcionar datos verificados sobre la seguridad de la piel. Las pruebas de biocompatibilidad son un requisito fundamental para la fabricación de dispositivos médicos. Los proveedores que carecen de esta documentación probablemente tienen sistemas de gestión de calidad inadecuados en todos los procesos de producción.

Lo que revela la documentación faltante
Un proveedor que no puede proporcionar informes de prueba ISO 10993 le está diciendo algo importante sobre su operación. O bien nunca realizaron las pruebas requeridas, o sus sistemas de control de documentos están tan desorganizados que no pueden localizar registros esenciales.
Ambos escenarios indican problemas sistémicos de calidad. Si se omitieron las pruebas de biocompatibilidad, ¿qué otros pasos de seguridad se omitieron? Si no se pueden localizar los registros, ¿cómo rastreará este proveedor los problemas de producción si surgen defectos más adelante?
Señales de alerta en las respuestas de los proveedores
Cuando evaluamos proveedores de componentes potenciales, ciertas respuestas desencadenan inmediatamente preocupación:
| Respuesta del proveedor | Lo que probablemente significa | Acción recomendada |
|---|---|---|
| "Nuestros materiales son de grado médico, no se necesitan pruebas" | Malentendido de los requisitos reglamentarios | Solicitar certificados de prueba específicos |
| "Podemos proporcionar documentos después de que usted ordene" | Los documentos pueden no existir; creación de informes falsos | Exigir informes antes del compromiso de compra |
| "Los clientes anteriores nunca pidieron esto" | Brechas en el sistema de calidad; procesos no probados | Considerar proveedores alternativos |
| "Las pruebas son demasiado caras para este punto de precio" | El recorte de costos compromete la seguridad | Aumentar el presupuesto o aceptar un mayor riesgo |
Evaluación de los sistemas de calidad de los proveedores
Más allá de los informes de seguridad de la piel, evalúe estos indicadores de calidad al calificar a los proveedores de máquinas de ondas de choque:
Certificación ISO 13485: Esta norma internacional especifica los requisitos de gestión de calidad para las organizaciones de dispositivos médicos. Los proveedores certificados mantienen procedimientos documentados para el control de diseño, la producción y la vigilancia posterior al mercado.
Trazabilidad de la fabricación: Los proveedores de calidad pueden identificar los lotes exactos de materiales, las fechas de producción y los resultados de las pruebas de cualquier dispositivo por número de serie. Esta trazabilidad se vuelve crítica durante las situaciones de retirada del mercado.
Acceso al historial de quejas: Los fabricantes de renombre comparten datos agregados de quejas que muestran el rendimiento del dispositivo en el uso en el mundo real. Los patrones de quejas relacionadas con la piel indican brechas en las pruebas.
Nuestra lista de verificación de calificación de proveedores
Cuando los clientes preguntan cómo evaluamos a nuestros propios proveedores de componentes, compartimos este proceso de verificación:
- Solicitar certificado ISO 13485 y verificar con el organismo de certificación
- Exigir informes de pruebas de biocompatibilidad específicos para componentes en contacto con el paciente
- Solicitar certificados de análisis de materiales de los proveedores de materias primas
- Revisar los datos de tendencias de quejas relacionadas con problemas cutáneos
- Realizar auditoría de fábrica centrada en sistemas de control de documentos
Los proveedores que superan los cinco puntos de control demuestran un compromiso de calidad más allá de las garantías verbales.
¿Requerir estos informes de seguridad reducirá el número de quejas que recibo de mis clientes del salón?
Nuestro equipo de atención al cliente rastrea los patrones de quejas en todas las líneas de productos. Los datos muestran una clara correlación entre la documentación de seguridad completa y la reducción de las quejas en campo. Los dispositivos con biocompatibilidad verificada superan consistentemente a aquellos con lagunas documentales.
Sí, exigir informes de seguridad de la piel probablemente reducirá las quejas de los clientes de su salón. Los dispositivos que se han sometido a pruebas de biocompatibilidad adecuadas experimentan menos reacciones adversas en la piel, lo que conduce a una mayor satisfacción del paciente y menos quejas relacionadas con el tratamiento que sus clientes del salón deben abordar.

Comprensión de las causas raíz de las quejas
Las quejas cutáneas de la terapia de ondas de choque suelen caer en estas categorías:
Reacciones inmediatas: Enrojecimiento excesivo, hinchazón o ardor durante el tratamiento. A menudo causado por geles de acoplamiento no probados o materiales de superficie de la pieza de mano que irritan la piel sensible.
Reacciones retardadas: Dermatitis de contacto que aparece 24-72 horas después del tratamiento. Generalmente indica sensibilización a los componentes del material, exactamente lo que detectaría la prueba ISO 10993-10.
Efectos acumulativos: Cambios en la piel que se desarrollan después de múltiples sesiones de tratamiento. Los datos de biocompatibilidad a largo plazo ayudan a predecir estas respuestas antes de que afecten a los pacientes de sus clientes.
Cómo las pruebas adecuadas previenen las quejas
Cuando los proveedores realizan pruebas exhaustivas de biocompatibilidad, identifican materiales problemáticos antes de la producción. Este enfoque proactivo elimina las fuentes de quejas en lugar de reaccionar ante fallos en el campo.
| Tipo de queja | Pruebas que lo previenen | Reducción esperada |
|---|---|---|
| Irritación de la piel durante el tratamiento | Pruebas de irritación (ISO 10993-10) | 70-80% |
| Reacciones alérgicas post-tratamiento | Pruebas de sensibilización (ISO 10993-10) | 60-70% |
| Cambios inusuales en la textura de la piel | Pruebas de citotoxicidad (ISO 10993-5) | 50-60% |
| Reacciones cutáneas relacionadas con el gel | Caracterización de materiales (ISO 10993-18) | 80-90% |
Apoyando a los clientes de su salón
Más allá de reducir la frecuencia de las quejas, la documentación de seguridad ayuda a los clientes de su salón a responder eficazmente cuando ocurren problemas. Proporcionarles resúmenes de pruebas de biocompatibilidad les permite tener conversaciones informadas con pacientes preocupados.
Los salones pueden explicar que los dispositivos se sometieron a una rigurosa evaluación de seguridad y que las reacciones leves y temporales se encuentran dentro de los parámetros normales documentados durante las pruebas clínicas. Esta transparencia genera confianza en el paciente y reduce la escalada a quejas formales.
Tendencias actuales de la industria
La Sociedad Internacional para el Tratamiento Médico con Ondas de Choque (ISMST) actualizó sus directrices, enfatizando la inspección de la piel posterior al tratamiento. Los profesionales deben monitorear los patrones de enrojecimiento que puedan indicar problemas con el dispositivo. Este mayor escrutinio hace que la documentación de seguridad verificada sea más valiosa que nunca.
Observamos una creciente demanda de "hojas de resumen de biocompatibilidad", documentos de una sola página que condensan informes de pruebas completos en formatos fáciles de usar para los profesionales. Estos resúmenes ayudan al personal del salón a comprender qué pruebas se realizaron sin revisar informes técnicos de laboratorio.
Impacto Empresarial a Largo Plazo
Reducir las quejas protege la reputación de su marca y fortalece las relaciones con los clientes. Los propietarios de salones que experimentan menos quejas de pacientes siguen siendo clientes leales. También se convierten en fuentes de referencia, recomendando sus dispositivos a colegas basándose en un rendimiento confiable.
El costo de las pruebas de seguridad integrales durante el abastecimiento es mínimo en comparación con la gestión de escaladas de quejas, el procesamiento de devoluciones y la reconstrucción de relaciones comerciales dañadas.
Conclusión
Requerir informes de pruebas de seguridad de la piel al adquirir máquinas de terapia de ondas de choque protege su marca, reduce la exposición a la responsabilidad y garantiza mejores resultados para los usuarios finales. Esta documentación no es opcional, es esencial para una importación responsable y el éxito comercial a largo plazo.
Notas al pie
1. Explica el papel fundamental del control de calidad para garantizar la seguridad y eficacia de los dispositivos médicos. ↩︎
2. Proporciona una descripción general de las normas internacionales para la evaluación de la biocompatibilidad de los dispositivos médicos. ↩︎
3. Proporciona una visión general completa de la terapia de ondas de choque extracorpóreas y sus usos médicos. ↩︎
4. Define la energía acústica como una forma de sonido utilizada en diagnósticos y terapéuticas médicas. ↩︎
5. Explica la norma ISO 10993 como el estándar clave y el marco integral para las pruebas de biocompatibilidad de dispositivos médicos. ↩︎
6. Define los dispositivos médicos de Clase II de la FDA como productos de riesgo moderado que requieren controles especiales para garantizar la seguridad y la eficacia. ↩︎
7. Reemplazado con una página de trabajo de BSI, un organismo de certificación autorizado, que detalla la certificación ISO 13485. ↩︎
8. Reemplazado con la página oficial de la tienda web de IEC para el estándar ISO 14971. ↩︎


